Alors que le monde se tourne vers des solutions énergétiques plus durables, la production d’hydrogène par électrolyse de l’eau s’impose comme l’une des technologies clés pour un futur décarboné. Au cœur de cette révolution énergétique trône la cellule électrolyseur, véritable composant fondamental capable de transformer l’électricité en hydrogène propre. Son rôle dépasse la simple séparation des molécules d’eau : il s’agit d’un système complexe où la maîtrise des processus électrochimiques, la performance des matériaux et l’optimisation de chaque composant interagissent pour maximiser l’efficacité énergétique de la production. Aujourd’hui, comprendre la cellule électrolyseur, c’est pénétrer au sein d’un univers technique fascinant qui mêle chimie, physique et ingénierie avancée. Ce savoir permet d’entrevoir comment cette solution peut contribuer à résoudre d’importants défis liés au stockage d’énergie et à la transition écologique.
La cellule électrolyseur ne se réduit pas à une simple boîte produisant de l’hydrogène ; elle constitue le cœur d’un système électrochimique rigoureusement conçu. Chaque élément y joue un rôle précis : anode, cathode, membrane échangeuse de protons, catalyseur – autant de composants essentiels qui gouvernent la séparation efficace de l’eau en hydrogène et oxygène. Ces substrats doivent fonctionner en parfaite harmonie, conciliant à la fois résistance mécanique, conductivité ionique et stabilité chimique sur le long terme. Leur combinaison permet également de limiter la recombinaison des électrons, un phénomène souvent problématique qui réduit le rendement global. Ainsi, en analysant en profondeur la cellule électrolyseur, on saisit mieux les leviers d’amélioration de la production d’hydrogène et l’évolution des technologies qui la supportent.
Fonctionnement détaillé de la cellule électrolyseur dans la production d’hydrogène
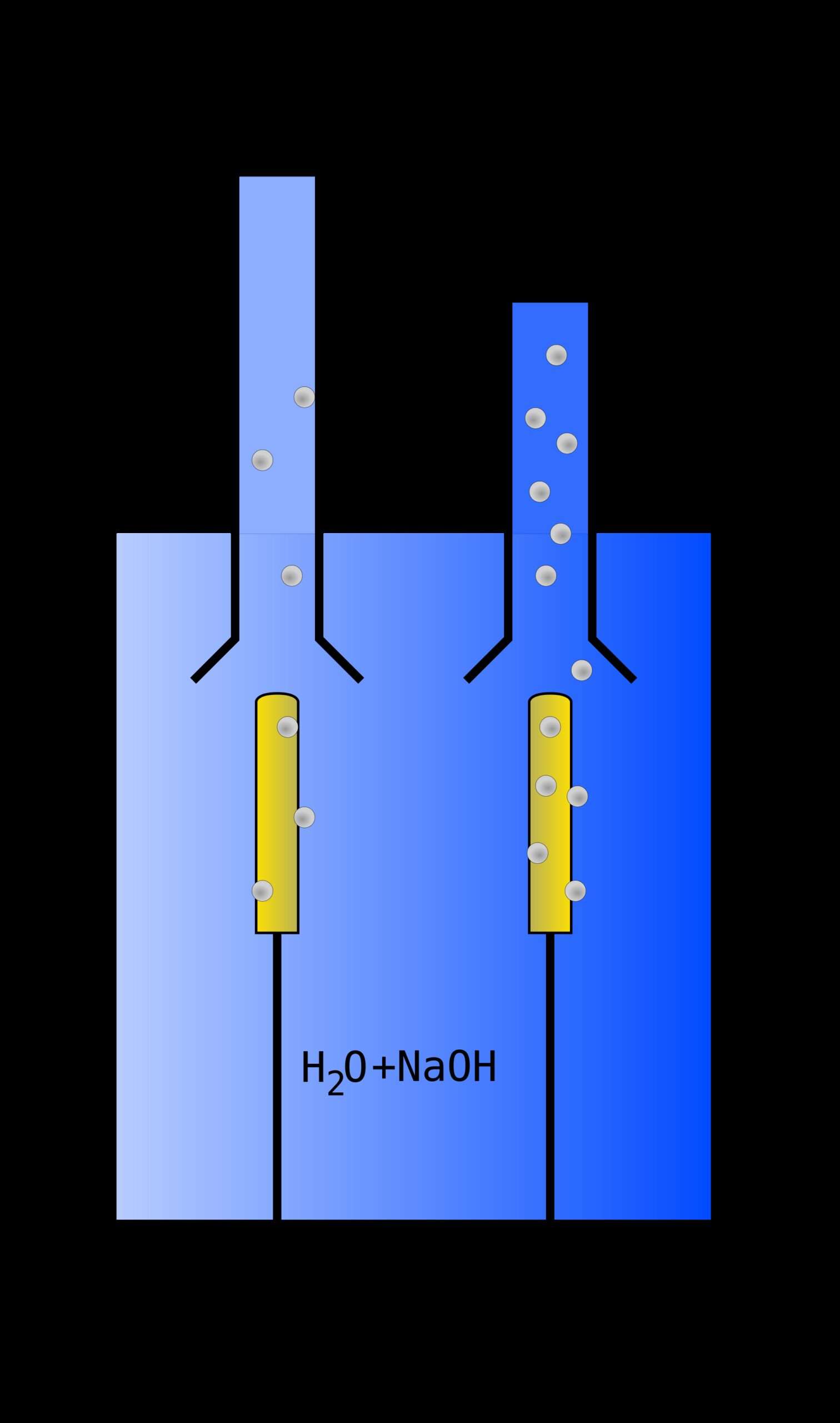
La cellule électrolyseur se compose principalement de deux électrodes : une anode et une cathode, séparées par une membrane échangeuse de protons. Cette membrane, souvent en Nafion ou autres polymères spécifiques, agit comme une barrière sélective qui ne laisse passer que les ions H+ (protons). Lorsque l’électricité est appliquée, l’électrolyse de l’eau démarre grâce à des réactions chimiques précises. À l’anode, l’eau est oxydée pour produire des protons, des électrons et du dioxygène. Ces protons traversent la membrane tandis que les électrons circulent dans un circuit externe vers la cathode où ils réagissent avec les protons pour former de l’hydrogène moléculaire.
Un point capital est la présence du catalyseur sur les électrodes, généralement à base de platine ou de matériaux moins coûteux comme le nickel pour les électrolyseurs alcalins. Ce catalyseur abaisse l’énergie d’activation des réactions électrochimiques, facilitant l’oxydation et la réduction sans surchauffer le système. Sans eux, l’efficacité énergétique de la cellule électrolyseur chuterait considérablement.
Un autre enjeu est la minimisation de la recombinaison des électrons avec les protons avant qu’ils ne puissent se recombiner en hydrogène. Cette recombinaison non souhaitée crée des pertes énergétiques. Le design et la qualité de la membrane, combinés à l’architecture interne, sont donc déterminants pour maintenir un haut rendement dans la production d’hydrogène.
Cette configuration peut être adaptée selon le type d’électrolyse. Par exemple, dans l’électrolyse alcaline, la membrane échangeuse de protons est souvent remplacée par une solution basique conductrice, alors que dans les électrolyseurs PEM (Proton Exchange Membrane), la fameuse membrane joue un rôle central. Le choix dépendra de la balance entre coûts, efficacité et durabilité recherchée.
Les matériaux clés et leur impact sur l’efficacité de la cellule électrolyseur
Le fonctionnement d’une cellule électrolyseur repose sur la qualité et les propriétés spécifiques de ses constituants. Les matériaux choisis pour l’anode, la cathode et la membrane sont déterminants pour le rendement, la durée de vie, et la robustesse du dispositif. Par exemple, un catalyseur performant comme le platine ou le ruthénium favorise la vitesse des réactions à l’anode et à la cathode, mais le coût peut rapidement devenir prohibitif pour une production à large échelle.
C’est pourquoi de nombreuses recherches en 2026 portent sur des alternatives moins onéreuses et plus abondantes, comme des alliages de nickel, du cobalt, voire des catalyseurs dits non-nobles à base de carbone dopé ou de matériaux nanostructurés. Ces innovations permettent non seulement d’abaisser les coûts, mais aussi d’améliorer la tolérance aux conditions agressives de l’électrolyse, notamment la corrosion et l’usure mécanique.
La membrane échangeuse de protons mérite une attention particulière. Fabriquée à partir de polymères spécifiques, elle doit combiner plusieurs fonctionnalités essentielles : perméabilité aux protons, imperméabilité aux gaz, résistance chimique et mécanique. Toute défaillance de la membrane peut entraîner une baisse de performance par mélange des gaz produits ou par augmentation de la résistance électrique.
Voici une liste des critères essentiels que doivent remplir les matériaux pour optimiser la cellule électrolyseur :
- Haute conductivité ionique pour faciliter le passage des protons via la membrane.
- Excellente résistance chimique face aux milieux corrosifs présents aux électrodes.
- Stabilité mécanique pour supporter la pression et les cycles de température.
- Catalyseurs peu coûteux mais efficaces pour réduire le coût global.
- Compatibilité entre matériaux de membrane et électrodes pour limiter les pertes.
Un tableau synthétique illustre les caractéristiques types des matériaux récemment utilisés dans les cellules électrolyseurs :
| Composant | Matériau | Avantages | Inconvénients |
|---|---|---|---|
| Anode | Platinium (Pt), Ruthénium (Ru) | Très bonne activité catalytique | Coût élevé, rareté |
| Cathode | Nickel, alliages Ni-Co | Coût modéré, bonne durabilité | Activité catalytique moindre que Pt |
| Membrane | Nafion, membranes PFSA | Perméabilité protonique élevée, robustesse | Sensibilité à la température, coût |
| Catalyseur alternatif | Carbone dopé, nano-oxydes | Faible coût, bonne durabilité | Réactivité parfois inférieure |
Ce panorama souligne comment l’équilibre entre performance et coûts doit être trouvé afin de démocratiser l’usage des cellules électrolyseurs, notamment dans des applications de stockage d’énergie à grande échelle.
Les enjeux énergétiques et environnementaux liés à la cellule pour électrolyseur
La production d’hydrogène par électrolyse est une des voies les plus prometteuses pour stocker efficacement l’énergie renouvelable intermittente, comme celle issue du solaire ou de l’éolien. Cependant, le succès de cette technologie dépend largement de la performance énergétique de la cellule électrolyseur elle-même. Une cellule peu efficace consomme trop d’électricité pour produire une quantité donnée d’hydrogène, ce qui remettrait en cause l’utilité écologique du procédé.
Dans ce contexte, plusieurs indicateurs permettent de mesurer la qualité des cellules :
- Le rendement électrochimique : quantifie la part de l’énergie électrique convertie en hydrogène.
- La densité de courant : correspond à la quantité d’hydrogène produite par unité de surface d’électrode.
- La durabilité : mesure la stabilité de la cellule sous fonctionnement prolongé sans perte de performance.
Ces paramètres sont fonction non seulement des matériaux utilisés, mais aussi de la gestion thermique, de la pression, et de l’alimentation électrique. Pour pallier les défis liés à la recombinaison des électrons et limiter les pertes, les ingénieurs conçoivent des architectures de cellule optimisées favorisant un transfert de charge rapide et un contact maximal des gaz générés avec les électrodes.
Par ailleurs, la production d’hydrogène vert via ces cellules est envisagée comme un pilier pour décarboner plusieurs secteurs, dont : la mobilité (hydrogène pour piles à combustible), l’industrie lourde (chimie, métallurgie), et le chauffage urbain. Le stockage d’énergie dans l’hydrogène permet ainsi de lisser la variabilité des renouvelables tout en réduisant l’émission de CO2.
Différents types de cellules électrolyseurs et leurs applications dans l’industrie
Il existe aujourd’hui plusieurs technologies de cellules électrolyseurs, chacune adaptée à des conditions spécifiques et des objectifs à atteindre :
- Cellules à électrolyse alcaline : utilisent une solution basique comme électrolyte. Elles sont robustes, peu coûteuses, et bien adaptées aux installations industrielles de grande taille.
- Cellules à membrane échangeuse de protons (PEM) : offrent un faible encombrement, une réponse rapide à la variation de charge et une haute pureté d’hydrogène. Elles sont privilégiées pour les applications mobiles et le stockage d’énergie décentralisé.
- Électrolyseurs à oxyde solide (SOEC) : fonctionnent à haute température, permettant un meilleur rendement énergétique théorique, mais avec des contraintes matérielles et d’usure plus marquées.
Le choix de la cellule électrolyseur dépendra des priorités, qu’elles soient économiques ou techniques. Malgré ça, le développement continu des catalyseurs et membranes améliore systématiquement l’efficacité et la durabilité de ces dispositifs.
En industrie, ces solutions contribuent à la production d’hydrogène pour :
- Alimentation des piles à combustible dans les transports lourds.
- Processus chimiques nécessitant du gaz hydrogène pur.
- Stockage d’énergie renouvelable sur sites isolés.
Maintenance et optimisation : clés pour une cellule pour électrolyseur performante
Maintenir la performance d’une cellule électrolyseur passe par la maîtrise de plusieurs aspects techniques. Premièrement, la maintenance régulière des électrodes et de la membrane est essentielle pour éviter la dégradation causée par la corrosion, l’accumulation de dépôts, ou la dégradation mécanique. Ces phénomènes augmentent la résistance interne, diminuent la conductivité ionique et donc amoindrissent la production d’hydrogène.
Ensuite, une bonne gestion thermique optimise les conditions électrochimiques : plus la température est stable et adéquate, plus la membrane conserve ses propriétés et les réactions sont plus efficientes. Un excès de chaleur, ou au contraire une température trop basse, impacte négativement la production d’hydrogène.
Les systèmes de contrôle électronique modernes mesurent en continu des paramètres comme la tension, le courant, la pression et la température. Ces données permettent d’ajuster précisément les conditions de fonctionnement pour éviter la recombinaison des électrons et maximiser le rendement.
Finalement, l’optimisation peut passer par le choix de nouveaux matériaux ou l’amélioration du design interne de la cellule. De nombreuses entreprises s’orientent vers la création de cellules modulaires, plus faciles à réparer et à remplacer, afin de favoriser une économie circulaire et réduire les déchets industriels.
Les critères clés pour garantir une cellule électrolyseur performante sont donc :
- Surveillance et nettoyage réguliers des électrodes et membranes.
- Contrôle rigoureux des températures et de la pression de fonctionnement.
- Utilisation de catalyseurs adaptés à l’évolution technologique.
- Gestion fine des conditions électriques pour éviter les pertes.
- Innovation dans le design pour faciliter l’entretien et allonger la durée de vie.
Qu’est-ce qu’une cellule électrolyseur ?
La cellule électrolyseur est le composant principal qui permet de diviser l’eau en hydrogène et oxygène par l’application d’un courant électrique, basé sur l’électrolyse de l’eau.
Pourquoi la membrane échangeuse de protons est-elle importante ?
Elle permet la séparation des charges en ne laissant passer que les protons, évitant le mélange des gaz et améliorant l’efficacité énergétique de la cellule.
Quels sont les principaux matériaux utilisés dans les électrodes ?
Les matériaux classiques sont le platine, le ruthénium pour l’anode, et le nickel ou ses alliages pour la cathode, parfois remplacés par des catalyseurs alternatifs pour réduire les coûts.
Comment éviter la recombinaison des électrons dans la cellule ?
Grâce à une membrane performante, un bon design de la cellule et un contrôle précis des conditions électrochimiques, il est possible de limiter cette perte d’énergie.
Quels sont les avantages des différents types d’électrolyseurs ?
Les électrolyseurs alcalins sont économiques et robustes, les PEM offrent une haute pureté d’hydrogène et une réponse rapide, tandis que les SOEC promettent un rendement énergétique élevé à haute température.